
Els projectes d’investigació clínica són essencials per poder descobrir noves maneres de tractar certes condicions oculars i millorar els tractaments actuals, sempre amb el focus a la seguretat, així com la salut i la qualitat de vida del/la pacient. Tanmateix, la investigació pot semblar inaccessible per a les persones que no formen part de la comunitat acadèmica o no disposen de coneixements específics d’oftalmologia.
És per això que a la nostra web tenim, per una banda, un llistat actualitzat dels projectes de recerca que estem duent a terme en aquests moments. I, a continuació, expliquem en què consisteixen els assaigs clínics, de quins tipus se’n poden fer i de quines fases consten. D’aquesta manera, qualsevol pacient que ho desitgi pot consultar els projectes actuals, veure si n’hi ha algun del qual es pugui beneficiar o fins i tot participar-hi de manera voluntària.
Es tracta d’un tipus d’investigació mèdica que pretén determinar si un tractament és segur i eficaç en persones. A més d’aquest objectiu principal (també anomenat endpoint primari), els assaigs clínics pretenen aportar més informació sobre el tractament analitzat (endpoint secundari).
Aquest tipus de projecte s’inicia a partir d’hipòtesis d’estudis in vitro, en animals, o estudis observacionals, en els quals es troba evidència parcial o raons per creure que el tractament estudiat pot presentar beneficis per a un cert grup de pacients.
Cada assaig clínic pot ser de diferents tipus i fases i té una durada variable (des de l’inici fins a la conclusió de l’estudi poden passar entre 7 i més de 20 anys).
Un assaig clínic pot constar de les següents fases:
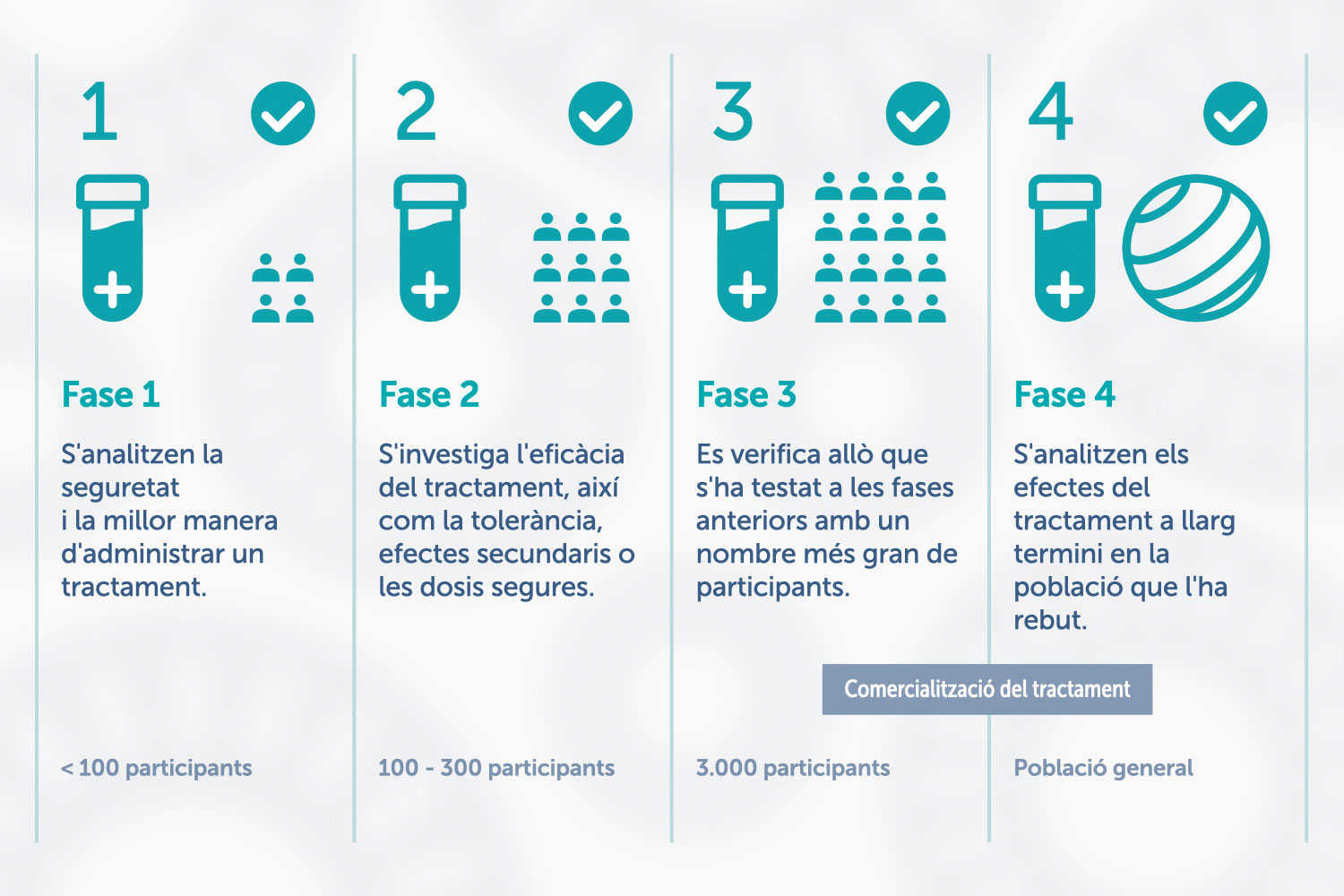
Hi ha molts tipus d’assaigs clínics, que poden ser de diferents tipus en funció de múltiples factors.

Foto de Kaboompics.com a Pexels.

Escriu-nos o demana hora amb el nostre equip mèdic.